Resumen: Para imitar a la evolución que muta y recombina organismos vivos, ahora un sistema quķmico artificial puede duplicarse con seis en vez de cuatro bloques constructivos.|
basado en una comunicación de la UF
Un equipo de cientķficos de la Universidad de Florida Han desarrollado, por vez primera, un sistema quķmico artificial que puede imitar el proceso evolutivo natural que experimentan los organismos vivos.
Ejemplos de estructuras tķpicas de polimeros. Crédito: Molecular Universe
|
Especķficamente, el equipo mostró que una molécula de casi-ADN creada artificialmente con seis nucleótidos estructurales – en vez de los cuatro que encontramos en el DNA natural – puede soportar el “fotocopiado” molecular conocido como reacción en cadena de la polimerasa (PCR). La molécula de casi-ADN dirige la sķntesis de copias de si misma y luego de copias de las copias imitando el proceso natural de la evolución, tal como fue inicialmente esbozada por Charles Darwin. Un nucleótido es un componente del ADN, o una “letra” del alfabeto genético usado para escribir el “libro” que describe nuestra herencia genética.
“Las implicaciones potenciales de esto en diagnostico y medicina son claras”, dice Steven Benner, un distinguido profesor de quķmica, anatomķa y biologķa celular, e investigador principal de este estudio. “Esta tecnologķa puede incrementar nuestra capacidad para detectar material genético no deseado de virus, bacterias o incluso agentes biológicos de uso militar. También puede racionalizar nuestra capacidad para detectar defectos en el ADN natural, como aquellos relacionados con cįncer o enfermedades genéticas”.
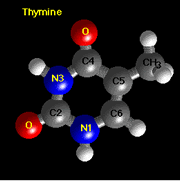
Estructura de la timina, una de las bases encontrada en el ADN y no en el ARN. Crédito: Richard B. Hallick
|
El artķculo, que aparecerį en la edición de esta semana en la revista Nucleic Acids Research, proporciona un punto clave hacia el desarrollo de formas de vida artificial. Los cientķficos han estado intentando conseguir un sistema quķmico artificial que soportara la evolución Darviniana durante una década.
Benner y Michael Sismour, un estudiante graduado de la UF, han profundizado en el trabajo hecho por James Watson y Francis Crick, los ganadores del premio Nóbel que propusieron hace 50 ańos la doble hélice de ADN. Watson y Crick mostraron que cuatro nucleótidos codificaban la información en la molécula de ADN, escribiendo nuestras instrucciones genéticas como una cadena de letras - G, A, T y C, que representan guanina, adenina, timina y citosina. Estas letras forman el famoso emparejamiento de Watson y Crick que mantiene las dos cadenas de la doble hélice. Este apareamiento sigue reglas muy sencillas: A de una cadena se empareja con T de la otra, y G de una se aparea con C de la otra.
Hace una década, en el Instituto Federal de Tecnologķa Suizo, el grupo de Benner demostró que era posible incrementar el nśmero de nucleótidos de cuatro a doce. Incluso parece ser mejor en el caso del ADN. La adición de nucleótidos extra incrementa el nśmero de reglas de apareamiento, segśn Benner. 'Esto incrementa las maneras en que el ADN puede aparearse, lo que incrementa enormemente el control de los biotecnólogos sobre como el ADN se integra”.
Este control incrementado ha permitido ensayos diagnósticos comercialmente rentables. Hoy en la clķnica, pacientes infectados con HIV y Hepatitis C tienen la carga de virus de su organismo monitorizada con herramientas diagnósticas que emplean los nucleótidos extra de Benner. Esto ayuda a los médicos a predecir precisamente cuando crece la probabilidad de generación de una cepa resistente del virus en un paciente.
La historia de una molécula de ADN esta esculpida en su estructura quķmica. Crédito: UIC
|
“Nuestro ADN artificial beneficia generalizadamente a los pacientes en la diagnosis”, dice Benner. “Sin embargo hasta ahora, ha sido totalmente pasivo. No ha sido capaz de copiarse”.
Con objeto de crear moléculas de casi-ADN capaces de duplicarse, los investigadores tenķan que encontrar una enzima, conocida como ADN polimerasa, que pudiera colocar los monómeros GATC del ADN natural en las posiciones necesarias para crear los famosos pares de bases de Watson-Crick. Luego unirķa los nucleótidos correctamente apareados en una cadena.
Segśn Benner, la adición de un quinto y un sexto nucleótido no fue difķcil desde la perspectiva quķmica. Pero fue difķcil encontrar la ADN polimerasa que aceptara estos nucleótidos no naturales.
“Las ADN polimerasas han evolucionado durante miles de millones de ańos para aceptar las cuatro letras naturales en el ADN – A, T, C y G. Convencerlas para que aceptaran dos nuevas letras, digamos K y X, fue complicado”.

Arbol evolutivo de las especies de primates dibujadas. Imagen completa. Crédito: Mark A. Klingler, Carnegie Museum of Natural History
|
Benner cambió a una nueva tecnologķa llamada “ingenierķa de proteķnas” para desarrollar una ADN polimerasa alterada que pudiera funcionar. Utilizando esta polimerasa modificada el equipo fue capaz de “evolucionar”su ADN artificial a los largo de cinco generaciones.
Como suele ocurrir el, el trabajo del grupo de la UF habķa sido anticipado por la ciencia ficción. En un episodio de la popular serie de TV “Expedientes X”, uno de los protagonistas encuentra en un virus un quinto y un sexto nucleótido – un nuevo par de bases – y declaraban: “Lo que vemos no existe en ningśn lugar en la naturaleza. Ha de ser, por definición, extraterrestre”.
O, por lo que parece, del laboratorio de Benner.
'Considerando lo duro que hemos tenido que trabajar para conseguir una polimerasa terrestre que aceptara nuestro ADN artificial, dudamos que éste pudiera sobrevivir un instante fuera del laboratorio en este planeta. Pero un ADN de seis letras podrķa sustentar vida en otro planeta, donde la vida comenzó con seis letras y le resulta familiar. O incluso la ADN podrķa contener

'...una pequeńa charca templada, con todo un muestrario de sales amónicas y fosfóricas, luz calor, electricidad, etc...”, Charles Darwin, en los orķgenes de la vida en charcas con oleaje. Crédito:Smithsonian
|
'Esto es un gran adelanto”, dice Christopher Switzer, que empezó este trabajo en el laboratorio de Benner en Suiza hace una década y que hoy es director del departamento de Quķmica en la Universidad de California en Riverside.
'La noticia es enormemente excitante”, dice Joseph Piccirilli, que también comenzó investigando en esta įrea, y que es ahora miembro del Instituto Médico Howard Hughes en la Universidad de Chicago. “Abre una nueva dirección en la interfase entre quķmica y biologķa”.
Steven A. Benner is a member of the NASA Astrobiology Institute (NAI).

