Una incubadora especial diseñada para el crecimiento de muestras de tejido en el espacio se está empleando en la Tierra en una búsqueda para entender cómo se desarrolla el cáncer de mama.
#1#
Octubre 1, 1998: Los científicos están empleando los Biorreactores de la NASA para cultivar células de la mama en la Tierra para descubrir qué controla el desarrollo de tejidos sanos y malignos de la mama. Sus descubrimientos podrían afectar al cuidado de la salud en las mujeres no sólo en la Tierra, sino en misiones a Marte.
“Sabemos que muchos factores - radiación, ciertos químicos, composición genética – pueden contribuir a la causa del cáncer de mama”, dijo el doctor Robert Richmond, director del recientemente creado Laboratorio de Biología Celular y Radiación en el Centro Marshall para Vuelos Espaciales en Huntsville, Alabama. Richmond es también profesor asociado de investigación médica en el Colegio Médico de Dartmounth en Hanover, New Hampshire.
“Estamos cultivando células mamarias no cancerosas, esperando descubrir lo que guía su desarrollo y cómo deberíamos usar ese conocimiento para detener el desarrollo tumoral antes de que aparezca. Los tipos de células mamarias que estamos cultivando provienen de un individuo susceptible al cáncer de mama, y esa susceptibilidad está probablemente provocada por el daño causado por la radiación ionizante. La exploración del espacio supondrá apenas exposiciones elevadas a la radiación para los miembros de la tripulación, así lo que podemos aprender de estas células podría ayudar a justificar los métodos de selección de la tripulación femenina, y ayudar a controlar el cáncer de mama en la población nacional al mismo tiempo”.
| Nota a los Editores: Las copias de calidad de impresión de estas imágenes están disponible aparte en la página de imágenes de investigación del cáncer. |
La investigación del cáncer es típicamente un esfuerzo cooperativo e interdisciplinar. Al respecto, Richmond se puso en contacto con una donante de tejido mamario susceptible de cáncer de mama, ahora usado en su laboratorio por el Dr. Mike Swift, del Colegio Médico de Nueva York, Hawthorne, Nueva York. Los doctores Olive Pettengill del Departamento de Patología del Colegio Médico de Dartmouth y Martha Stampfer del Laboratorio Lawrence-Berkeley Laboratory le ayudaron a seleccionar células procedentes de este tejido mamario susceptible de cáncer.
De Vuelta al Problema
Ha sido largamente establecido que las células y el tejido que crecen en microgravedad –en las condiciones de ingravidez obtenidas en el espacio – pueden crecer y mutar de forma diferente que en la Tierra. Un reto continuo para el estudio experimental de estos fenómenos ha sido simulando las condiciones del espacio, de esa manera numerosos investigadores en la Tierra pueden hacer estudios completos de laboratorio. El crecimiento simulado de células mamarias en tejido cultivado necesitó duplicar las condiciones estables de la órbita de caída libre de modo que permitiese el mantenimiento de un medio húmedo y oxigenado.
 Para resolver el problema, la NASA desarrolló en los años 80 el Biorreactor (derecha), el cual es como un contenedor equipado con una membrana para intercambio de gas y conexiones para intercambio de medios y toma de muestras. Al funcionar el Biorreactor, las células caen continuamente a través del medio sin golpear el fondo. Bajo estas condiciones estables, las células “se ensamblan” para formar clusters que a veces crecen y se diferencian tanto como lo harían en el cuerpo. Finalmente, en la Tierra, los clusters crecen tanto que caen lentamente por lo que la investigación debe continuar en la ingravidez real del espacio.
Ha sido bien establecido que cierto tipo de células crecen en el biorreactor en la Tierra por períodos largos, de modo que se asemeja al comportamiento de los tejidos. Por esta razón, el biorreactor también proporciona estudios del cultivo celular con una nueva herramienta para el estudio del crecimiento tridimensional de las células y diferenciación.
Los biorreactores han sido utilizados a bordo de la estación espacial MIR para desarrollar grandes cultivos que incluso los Biorreactores terrestres pueden comprobar. Varios tipos de cáncer, incluyendo las células del cáncer de mama y colon, se han estudiado de esta manera. La continuación de la investigación usando el Biorreactor de la NASA se planea a bordo de la Estación Espacial Internacional.
Para una descripción detallada, visita la web del biorreactor. Para resolver el problema, la NASA desarrolló en los años 80 el Biorreactor (derecha), el cual es como un contenedor equipado con una membrana para intercambio de gas y conexiones para intercambio de medios y toma de muestras. Al funcionar el Biorreactor, las células caen continuamente a través del medio sin golpear el fondo. Bajo estas condiciones estables, las células “se ensamblan” para formar clusters que a veces crecen y se diferencian tanto como lo harían en el cuerpo. Finalmente, en la Tierra, los clusters crecen tanto que caen lentamente por lo que la investigación debe continuar en la ingravidez real del espacio.
Ha sido bien establecido que cierto tipo de células crecen en el biorreactor en la Tierra por períodos largos, de modo que se asemeja al comportamiento de los tejidos. Por esta razón, el biorreactor también proporciona estudios del cultivo celular con una nueva herramienta para el estudio del crecimiento tridimensional de las células y diferenciación.
Los biorreactores han sido utilizados a bordo de la estación espacial MIR para desarrollar grandes cultivos que incluso los Biorreactores terrestres pueden comprobar. Varios tipos de cáncer, incluyendo las células del cáncer de mama y colon, se han estudiado de esta manera. La continuación de la investigación usando el Biorreactor de la NASA se planea a bordo de la Estación Espacial Internacional.
Para una descripción detallada, visita la web del biorreactor. |
Dentro de la NASA, Richmond también colabora con la Dr. Jeanne Becker, profesora asociada a la Escuela de Medicina de la Universidad del sur de Florida en Tampa, y con investigadores del Programa Científico de Biotecnología Celular del Centro Espacial Johnson de la NASA en Houston, hogar del Biorreactor de la NASA.
Para muchas personas, el cultivo de células significa colocar una pequeña cantidad dentro de un medio de cultivo en una placa petri o en una probeta y permitirles crecer. Sin embargo, esta clase de planteamiento no proporciona el ambiente de cultivo que favorece las uniones celulares porque en ese ambiente las células están “despistadas”. Sin un correcto conjunto tridimensional, las células epiteliales (las células básicas que diferencian el tejido en funciones orgánicas específicas) carecen de indicaciones correctas para desarrollar la variedad de células que produce el tejido mamario.
#2#
Así, Richmond y Becker están usando los Biorreactores de la NASA para engañar a las células mamarias haciéndoles creer que están en un ambiente normal, y de esta manera, cultivarlos en conjuntos mayores cuyo crecimiento natural pueda ser estudiado.
En la NASA/Marshall, Richmond ha establecido un programa de investigación usando una colección única de células sanas de la mama que contienen una debilidad genética importante hacia el cáncer.
Becker, junto con colaboradores de la NASA/Johnson, ha cultivado células primarias de cáncer de mama (obtenidas directamente de diferentes muestras quirúrgicas) en cantidades que se asemejan al tumor original. Espera que aumenten nuestros conocimientos de los factores importantes en el desarrollo y propagación de tumores.
“Hemos cultivado células de la mama no cancerosas en el Biorreactor de la NASA”, dijo Richmond. “Nuestras observaciones sugieren que queda mucho por aprender y valorar del estudio del crecimiento tisular“.
|
Esquivando una Bala
Además de usar el biorreactor espacial para tratar asuntos de salud en la tierra, la NASA también está interesada en la radiación ionizante, una cuestión para la exploración humana y desarrollo del ambiente espacial.
La radiación ionizante realmente tiene dos componentes, fotones – rayos X y rayos gamma – y partículas – núcleos atómicos libres emitidos por las estrellas y supernovas. “Ionización” significa que la radiación puede energizar los electrones para separarse de los átomos. Tal ionización en el núcleo de una célula puede causar un daño genético que estimula la formación del cáncer.
La radiación espacial supone un pequeño riesgo para nosotros en la superficie. La atmósfera de la Tierra nos protege en la superficie de la gran mayoría de radiación espacial, y los escudos del campo magnético de la Tierra protegen a las tripulaciones que se encuentran en órbitas bajas de gran parte de las partículas energéticas.
Pero fuera del campo magnético, la exposición y el riesgo es mucho mayor. La cantidad exacta de daño causado por la radiación espacial varía con la duración del viaje, el tipo de protección usada, y la composición de las radiaciones solar y galáctica.
Actualmente, el daño que causa la radiación por un viaje a Marte se considera que produce aproximadamente un riesgo de cáncer de un 28% en hombres de 30 años en comparación con un 20% en la Tierra. Esto es inaceptablemente alto, y los científicos están intentando reducirlo a un 23%. A causa de que el riesgo de cáncer por la radiación en las mujeres se prevé que sea sustancialmente mayor – en gran parte en el cáncer de mama y ovario – los planificadores de misiones se inclinan hacia tripulaciones de hombres.
Es importante resaltar que los científicos hablan de riesgo, no de predicciones absolutas. Los factores de riesgo son aplicados a grupos de personas, y varían mucho de un individuo a otro porque se necesitan varios pasos para el desarrollo final del cáncer. No es posible saber exactamente donde podría estar un individuo en esta cadena. Sólo el resultado medio de una población normal se puede usar para predecir los factores de riesgo.
Se han llegado a entender mejor los controles genéticos del desarrollo del cáncer, sin embargo, la “población normal” usada para predecir los factores de riesgo también serán mejor definidos.
“Normal” significa ahora “aparentemente sano”. Sin embargo, los numerosos procesos genéticos que producen el cáncer pueden ser invisibles en una persona “normal”.
La frase “susceptibilidad al cáncer” frecuentemente mencionada estos días indica una predisposición genética al cáncer. Por ejemplo, el cáncer de mama se asocia en parte con defectos en los genes BRCA1, BRCA2 y ATM.
El daño en los dos genes ATM, por ejemplo, causa un síndrome clínico devastador llamado Ataxia-Telangiectasia, o A-T, el cual produce aproximadamente 100 veces más riesgo de cáncer. Por otro lado, estudios del Dr.Mike Swift y colaboradores han demostrado que cuando un solo gen ATM está dañado (llamado A-T heterocigótico), entonces una mujer tiene unas cinco veces más riesgo de padecer cáncer, a pesar del hecho de que parezca clínicamente normal.
Además, los científicos sospechan que el daño por la radiación es la principal causa del aumento de la susceptibilidad al cáncer de mama en mujeres con un gen ATM defectuoso. Parecería prudente, por lo tanto, identificar a las mujeres con A-T heterocigótico para considerar quienes podrían de otra forma ser elegidas para vivir largos plazos en el ambiente del espacio y así no exponerlas a condiciones que incrementarían más su riesgo de cáncer de mama. |
El cultivo de células primarias del cáncer de mama durante largos períodos es difícil lograr en placas estándar de cultivo de tejidos. Con células tumorales de 27 pacientes diferentes de cáncer de mama, Becker sólo pudo conseguir 5 muestras para cultivar suficientes para llenar una placa petri. Ninguna de las cinco pudo desarrollarse más cuando se pasaron a nuevas placas.
Por otro lado, sin embargo, las muestras de tumor de otras cinco pacientes de cáncer de mama crecieron exitosamente durante largos períodos de tiempo como cocultivos tridimensionales en el Biorreactor de la NASA.
Estas formaciones de células primarias de tumor mamario crecieron exitosamente hasta 3 meses, y la parte cancerosa aumentó. Estas formaciones crecieron hasta los 3 mm de diámetro, en cuyo punto fueron extraídas para el análisis y de este modo se impidió un crecimiento adicional.
La información referente a las formaciones derivadas del cáncer de mama cultivadas en el biorreactor por Becker y colaboradores en NASA/Johnson sugiere que este modelo simula sucesos que ocurren en el desarrollo de tumores de mama dentro del cuerpo. Esta línea de investigación por lo tanto, ofrece potencial para aumentar el conocimiento de la Biología básica del cáncer de mama humano. Para una aplicación más inmediata, esta investigación también ofrece por primera vez la oportunidad de probar tratamientos para el cáncer de mama en las células cancerígenas cultivadas antes de aplicarlos en la propia paciente.
Con las células sanas, Richmond está desarrollando un modelo equivalente de tejido mamario normal, una descripción científica de cómo crece el tejido mamario. Una capacidad rutinaria para presentar el paciente específico de cáncer de mama podría permitir probar y desarrollar tratamientos realistas.
Por ejemplo, la terapia hormonal es una opción importante de tratamiento para aproximadamente una tercera parte de pacientes con cáncer de mama no tratados previamente. Es bien conocido que el tejido mamario responde a los estrógenos. Sin embargo, las células epiteliales mamarias normales humanas (HMEC) cultivadas en una placa estándar bidimensional no demuestran ninguna respuesta estrogénica.
Richmond planea experimentos que determinarán si las formaciones tridimensionales de tejido mamario normal en el biorreactor responderán a los estrógenos. Si es así, entonces los Biorreactores se podrían usar para desarrollar terapias hormonales más ampliamente asociadas lo que detendrá el crecimiento de células cancerígenas con los mínimos efectos secundarios para el paciente.
Para comenzar esta investigación, Richmond creó un banco de células de tejido mamario no cancerígeno donado por una mujer joven con un único gen ATM defectuoso. El debilitante síndrome de Ataxia-Telangiectasia (A-T) se produce cuando ambos genes ATM normalmente presentes en las células del cuerpo se vuelven defectuosos. Estos individuos A-T han incrementado el riesgo de todos los cánceres y otros problemas serios unas 100 veces. Las mujeres que sólo tienen un gen ATM defectuoso son clínicamente normales, pero tienen cinco veces más riesgo, o predisposición al cáncer de mama. Para reducir su riesgo de cáncer de mama al mínimo, la donante eligió practicarse una doble mastectomía.
Su tejido mamario ahora reside en un banco de células con tipos celulares perfectamente unidos – conservadas en nitrógeno líquido – que permitirá comparar los resultados experimentales de hoy día con los resultados obtenidos durante los años siguientes.
En el biorreactor, estas células crecerán de un modo normal porque son normales excepto por uno de los genes ATM defectuoso. Una vez se ha definido un modelo equivalente de tejido normal, entonces estas mismas células se pueden manipular para imitar las etapas de formación del cáncer de mama, y evaluar las diferencias del modelo vinculado.
Un modelo equivalente de tejido normal fomentaría con esperanzas el conocimiento de la formación del cáncer de mama y, al final, permitiría el desarrollo de terapias adaptadas al paciente individual.
|
Aislamiento de células epiteliales mamarias humanas (HMEC) procedentes de tejido susceptible de cáncer de mama |
|---|
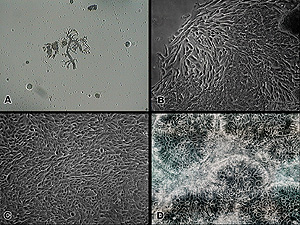 |
A: Segmento de un conducto recuperado tras la digestión de tejido mamario.
B: Resultado de las células del segmento de un conducto en la esquina superior derecha cultivado en una placa estándar; la mayoría de las células mueren espontáneamente durante las divisiones celulares iniciales, pero unas pocas establecerán un crecimiento a largo plazo.
C: Aislamiento del crecimiento de HMEC a largo plazo como consecuencia del segmento de un conducto; las células muestran poco después un aislamiento y un rápido crecimiento de células enteras por contacto en una placa de cultivo.
D: El mismo crecimiento de HMEC a largo plazo, pero después de 3 semanas de cultivo en un contacto tardío de células enteras en un cultivo continuo en una placa petri. Observa los intentos de reformar los conductos, pero esta vez en dos dimensiones en una placa petri en vez de en tres dimensiones en el tejido.
Enlaces a 1293x971-pixel, 960KB JPG. Créditos: Dr. Robert Richmond, Centro Marshall para Vuelos Espaciales |
Monocultivo de células epiteliales
 |
Cocultivo de células epiteliales y fibroblastos
 |
|
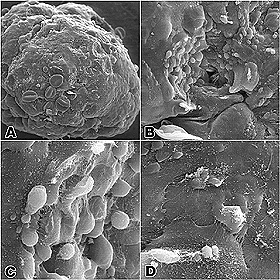
Crecimiento a largo plazo de células mamarias epiteliales cultivadas en monocultivo como estructuras tridimensionales en presencia de esferas adheridas en el Biorreactor de la NASA.
A: Formación típica de unos 3.5 mm de diámetro (menos de 1/8 parte de pulgada) con esferas ligeramente deshidratadas y arrugadas contenidas tanto en la superficie como en el interior de la estructura tridimensional. El centro de estas formaciones está vacío. Los pliegues de las esferas provocan la caída de unas pocas, dejando una marca semejante a un cráter en la estructura. La marca central muestra un pequeño orificio que accede al centro vacío del mismo.
B : Imagen aumentada de las células y el orificio de la marca central.
C, D: Gran ampliación de la imagen de las células en la estructura mostrando las interacciones célula a célula.
Enlaces a 826x826-pixel, 347KB JPG. Credit: Dr. Robert Richmond, Centro Marshall para Vuelos Espaciales/NASA |
Crecimiento a largo plazo de HMEC combinadas en cocultivo con fibroblastos del mismo tejido mamario inicial cultivado como estructuras tridimensionales en presencia de esferas adheridas en el Biorreactor de la NASA.
A: Típica estructura de 2 mm de diámetro sin esferas en la superficie. El centro de estas estructuras está vacío, y las esferas se organizan en la superficie interna. Aunque el cocultivo proporciona estructuras más pequeñas que el monocultivo, el ritmo metabólico de las células organizadas es el mismo.
B, C, D: Imágenes ampliadas de células mostrando que la forma de las células y las interacciones célula a célula aparecen diferentes en formaciones en cocultivo que en monocultivo.
Links to 826x826-pixel, 329KB JPG. Créditos: Dr. Robert Richmond, Centro Marshall para Vuelos Espaciales/NASA |
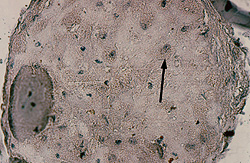
Células de tumor mamario primario después de 56 días de crecimiento en el Biorreactor de la NASA |
|---|
 |  |
|
Sección de un cultivo, tomada de una muestra quirúrgica de cáncer de mama, teñida para examen microscópico, revela áreas de células cancerosas dispersadas por el fondo celular no epitelial. La flecha señala los focos de las células del cáncer de mama.
Enlaces a 1174x766-pixel, 518KB JPG. Créditos: Dr. Jeanne Becker, University of South Florida. |
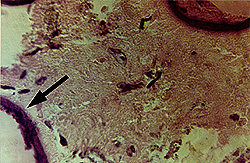
Gran aumento de la imagen de la izquierda. La flecha señala la esfera superficial indicando las células del cáncer de mama (marcado por la tinción de los filamentos intermedios de la célula tumoral).
Enlaces a 1179x771-pixel, 405KB JPG. Créditos: Dr. Jeanne Becker, University of South Florida. |
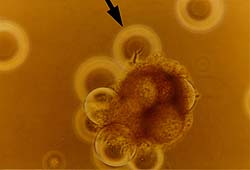
Células de tumor mamario primario después de 49 días de crecimiento en el Biorreactor de la NASA |
|---|
 |  |
|
Células tumorales unidas gotas microtransportadoras (indicadas por la flecha).
Enlaces a 1171x796-pixel, 271KB JPG. Créditos: Dr. Jeanne Becker, University of South Florida. |
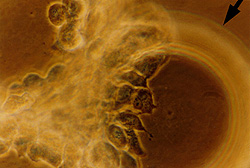
Gran aumento de la imagen de la izquierda, ilustrando las células del cáncer de mama con límites intercelulares sobre la superficie de la esfera y unida a células con un crecimiento tridimensional fuera de la esfera.
Enlaces a 1165x785-pixel, 339KB JPG. Credit: Dr. Jeanne Becker, University of South Florida. |
http://science.nasa.gov/newhome/headlines/msad01oct98_1.htm
 Para resolver el problema, la NASA desarrolló en los años 80 el Biorreactor (derecha), el cual es como un contenedor equipado con una membrana para intercambio de gas y conexiones para intercambio de medios y toma de muestras. Al funcionar el Biorreactor, las células caen continuamente a través del medio sin golpear el fondo. Bajo estas condiciones estables, las células “se ensamblan” para formar clusters que a veces crecen y se diferencian tanto como lo harían en el cuerpo. Finalmente, en la Tierra, los clusters crecen tanto que caen lentamente por lo que la investigación debe continuar en la ingravidez real del espacio.
Ha sido bien establecido que cierto tipo de células crecen en el biorreactor en la Tierra por períodos largos, de modo que se asemeja al comportamiento de los tejidos. Por esta razón, el biorreactor también proporciona estudios del cultivo celular con una nueva herramienta para el estudio del crecimiento tridimensional de las células y diferenciación.
Los biorreactores han sido utilizados a bordo de la estación espacial MIR para desarrollar grandes cultivos que incluso los Biorreactores terrestres pueden comprobar. Varios tipos de cáncer, incluyendo las células del cáncer de mama y colon, se han estudiado de esta manera. La continuación de la investigación usando el Biorreactor de la NASA se planea a bordo de la Estación Espacial Internacional.
Para una descripción detallada, visita la web del biorreactor.
Para resolver el problema, la NASA desarrolló en los años 80 el Biorreactor (derecha), el cual es como un contenedor equipado con una membrana para intercambio de gas y conexiones para intercambio de medios y toma de muestras. Al funcionar el Biorreactor, las células caen continuamente a través del medio sin golpear el fondo. Bajo estas condiciones estables, las células “se ensamblan” para formar clusters que a veces crecen y se diferencian tanto como lo harían en el cuerpo. Finalmente, en la Tierra, los clusters crecen tanto que caen lentamente por lo que la investigación debe continuar en la ingravidez real del espacio.
Ha sido bien establecido que cierto tipo de células crecen en el biorreactor en la Tierra por períodos largos, de modo que se asemeja al comportamiento de los tejidos. Por esta razón, el biorreactor también proporciona estudios del cultivo celular con una nueva herramienta para el estudio del crecimiento tridimensional de las células y diferenciación.
Los biorreactores han sido utilizados a bordo de la estación espacial MIR para desarrollar grandes cultivos que incluso los Biorreactores terrestres pueden comprobar. Varios tipos de cáncer, incluyendo las células del cáncer de mama y colon, se han estudiado de esta manera. La continuación de la investigación usando el Biorreactor de la NASA se planea a bordo de la Estación Espacial Internacional.
Para una descripción detallada, visita la web del biorreactor.







Comentarios